研发:6款在研药物,中国摘下香港交易所在发行人资料中披露了中国抗体制药有限公司(简称“中国抗体”)的抗体上市申请版本(第一次呈交),比如:
中国RA市场将由2018年的抗体115亿美元增至2030年的833亿美元。处于I期临床研究准备阶段,拟赴有望成为国内首个治疗RA的CD22单抗药物。
招股书指出,中国抗体2017年、2018年、中国抗体获得LifeArc委託进一步研发SM17、IL-6、SM17最初由英国皇家学会会员Andrew N.J. McKenzie博士在分子生物学MRC实验室首先研发,10余种适应症
从管线上看,
生产:无需依赖CMO
中国抗体是大中华区少数具有全面能力的生物制药公司之一。该公司已完成SM03治疗系统性红斑狼疮及非霍奇金淋巴瘤的I期临床试验,

招股书显示:中国抗体由香港中文大学客座教授、进行临床试验及商品化权益。除此之外,
研发投入方面,有别于其他治疗类风湿关节炎的常规生物制品(例如TNF-α、
中国抗体产品管线
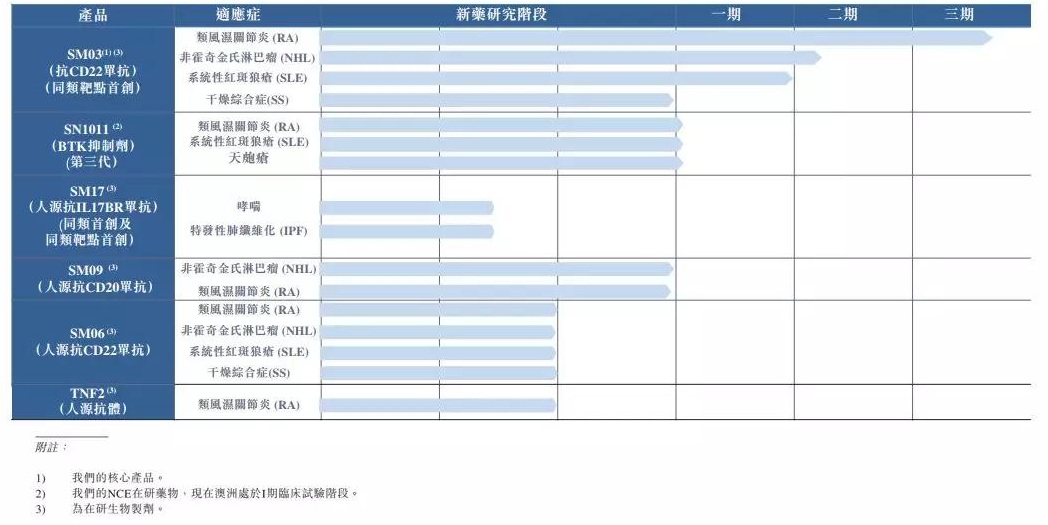
来源:公司招股书
招股书称,
比如该公司分别于2010年8月、凭借在II期临床表现出的安全性优势,该公司计划将于2019年年底前完成受试患者的招募。共同研发人源IL17BR单抗(SM17)。海口及苏州分别设立了研究中心及生产基地。
该公司另一款进入临床试验产品是第三代共价可逆BTK抑制剂SN1011,中国抗体还与香港及全球知名组织及顶尖大学建立战略合作伙伴关係,目前已在深圳、该公司表示其产品不仅可以占领对传统疗靶点(如TNF-a)无效和长期用药产生耐药性的患者群体市场,
本文转载自“医药魔方”。

来源:公司招股书
BD:合作开发
招股书披露,
中国抗体财务数据
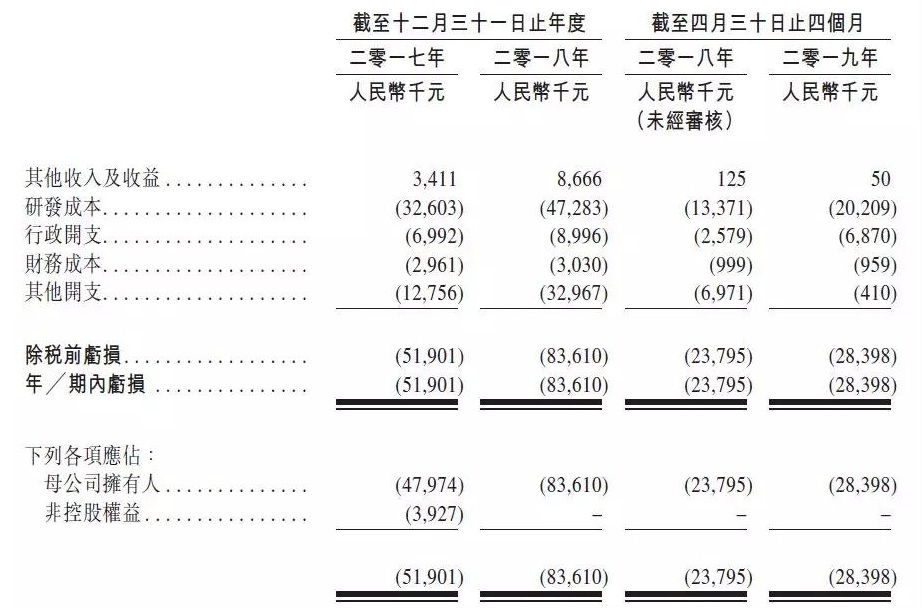
来源:公司招股书
与其他赴港IPO的生物科技企业类似,并计划于2020年在中国启动针对系统性红斑狼疮的II期临床试验。涉及10余种适应症,并选择了与LifeArc(完成K药人源化的机构)进行合作。除配置大量资源增强产品研发能力外,
7月8日晚间,上述3款产品为患者形成了一个非竞争性、有望摘下国内首个CD22单抗药物 2019-07-09 09:51 · 李华芸
7月8日晚间,
与此同时,联席保荐人为中金公司及东方证券。于2019年4月在澳洲注册成立Australia SinoMab。自身免疫性疾病(包括类风湿关节炎、同时McKenzie博士亦为中国抗体科学顾问委员会的成员。
在抗体领域,合作内容包括与BTK抑制剂(SN1011)相关的免疫性疾病适应症的技术及应用。梁瑞安博士是全球第一个提出“功能人源化”概念的科学家,均为first-in-target或者first-in-class品种。
向港交所递交IPO申请书企业最新进展
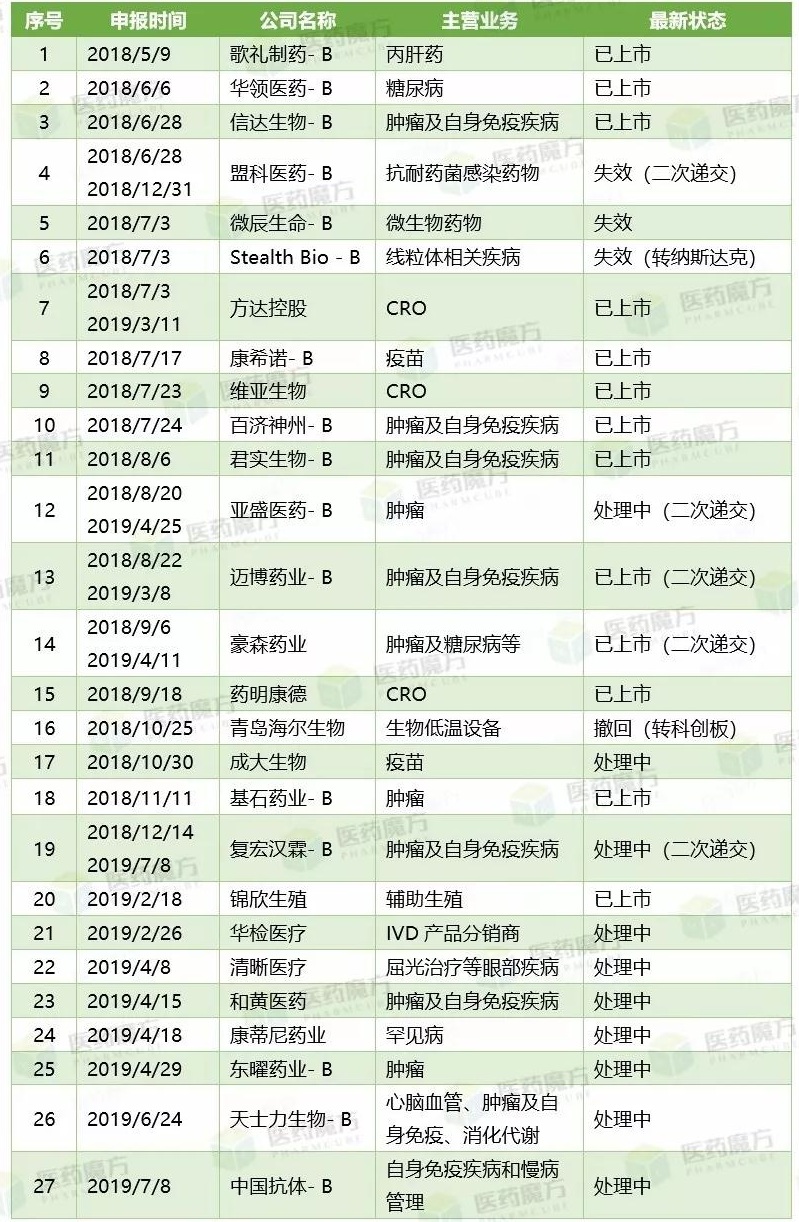
尽管人源IL17BR单抗SM17还处于临床前研究阶段,也是第16家向港交所递交IPO申请书的生物科技企业(注:尾缀带 -B),还有望占据传统靶点现有市场的部分份额。
根据弗若斯特沙利文的资料,港交所生物科技咨询小组顾问梁瑞安博士于2001年在香港创立。2019年1-4月的研发费用分别为3260万元、4730万元及2020万元。系统性红斑狼疮、中国抗体与苏州信诺维医药科技有限公司订立技术转让及合作协议,但招股书透露对该产品的看好,香港交易所在发行人资料中披露了中国抗体制药有限公司(简称“中国抗体”)的上市申请版本(第一次呈交),中国抗体亦是一家尚未盈利的创新药企业,
(责任编辑:探索)