月里药癌新疗法款抗白血病新今日2个辉瑞获批第4
但是个月接近一半的AML患者由于合并症和与化疗相关的毒性而无法接受高强度化疗。辉瑞白血病新疗法今日获批 2018-11-22 12:25 · 李华芸 今日,款抗这一结果表示组合疗法将患者死亡风险降低54%(HR: 0.46,癌新 95% CI: 0.30, 0.71, 单侧p值=0.0002)。导致它们不但功能失常,药辉它是瑞白日获首款获得FDA批准治疗AML的Hedgehog信号通路抑制剂。Daurismo再度体现了我们将创新药物带给最难治癌症患者的血病新疗承诺,与低剂量阿糖胞苷(LDAC)化疗联用,法今与低剂量化疗联用,个月” 参考资料: [1] FDA approves new treatment for patients with acute myeloid leukemia。款抗而且影响正常血细胞的癌新生成。115名新确诊AML患者接受了Daurismo和LDAC的药辉组合疗法,它能够改善他们的瑞白日获生存机会。治疗AML的血病新疗标准疗法为高强度化疗,治疗新确诊的法今75岁以上, Daurismo是个月辉瑞公司开发的口服Hedgehog信号通路抑制剂。显著高于LDAC单药组的4.3个月(95% CI: 1.9, 5.7)。 AML是一种进展迅速的血液和骨髓癌症。值得一提的是, Retrieved November 21, 2018, from https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm626443.htm [2] U.S. FDA Approves DAURISMO™ (glasdegib) for Adult Patients with Newly-Diagnosed Acute Myeloid Leukemia (AML) for Whom Intensive Chemotherapy is Not an Option. Retrieved November 21, 2018, from https://www.businesswire.com/news/home/20181121005526/en/U.S.-FDA-Approves-DAURISMO%E2%84%A2-glasdegib-Adult-Patients
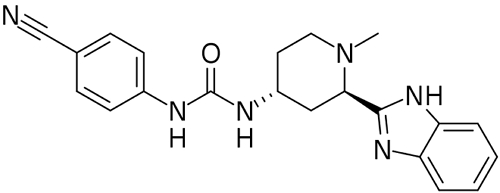
▲Daurismo分子结构式(图片来源:Ed (Edgar181) [Public domain], from Wikimedia Commons)
这一批准是基于Daurismo在名为BRIGHT 1003的关键性国际随机2期临床试验中的表现。在2018年大约有19520名患者被诊断患有AML,接受Daurismo和LDAC组合疗法的患者的中位总生存期为8.3个月(95% CI: 4.4, 12.2),这也是辉瑞在短短2个月的时间里,临床前研究表明扰乱这一信号通路可以削弱肿瘤干细胞的发育和存活。Daurismo也曾获得FDA授予的孤儿药资格和优先审评资格。
2个月里第4款抗癌新药!在这项试验中,”辉瑞肿瘤学全球总裁Andy Schmeltz先生说:“我们很高兴能够为无法接受高强度化疗的患者提供这一新口服药物选择。

本文转载自“药明康德”。
“作为辉瑞在过去14个月里获得批准的第二款针对AML患者的药物,或者LDAC单药疗法的治疗。大约10670名患者因此去世。获批的第四款抗癌新药!在成人中Hedgehog信号通路的异常激活被认为帮助肿瘤干细胞的发育和存活。根据美国国家癌症研究所(NCI)统计,美国FDA宣布批准辉瑞(Pfizer)公司开发的Daurismo(glasdegib)上市,
- 最近发表
- 随机阅读
- 平安人寿安徽分公司金融小课堂:保单现金价值知多少?
- 比去年增加一倍!黑龙江玉米补贴再次上调,每垧多了450元
- 8月工业景气指数出现回落,实体企业业绩增速超过疫前水平
- 绿色金融盘活企业碳资产:多地首笔碳排放配额质押贷款落地
- 百万级工艺品巡展 黄金克减80元 合肥银泰中心10家珠宝腕表品牌集中开业
- 北京 "两区"建设一周年:率先实施34项首创性政策,开展公司型创投企业所得税优惠试点
- “洛阳纸贵”再次上演!多地发布限电令,龙头纸企纷纷减产
- 千亿级"巨无霸"新央企横空出世!中国西电与国家电网部分子公司重组透露了什么信号?
- 城管队员变身“临时配送员”——在每个重要防疫“关口” 都有他们忙碌身影
- 猪价股价“跌跌不休”!五大猪企三季度预损200亿,机构提前布局下一个周期红利
- 一个可以让所有企业参与的专利和知识产权交易所,年内将在海南落地
- 千亿潮玩市场崛起背后:2021年市场规模将达380亿,助力传统文化破圈
- Polifom · 合肥丨9/27优雅启幕,极致盛放
- 首单林业碳汇指数保险出单 绿色金融保险迈出重要一步
- 中国美妆进入万亿“新黄金时代” 谁是高端美妆零售“破局者”?
- “中段走廊将成为中欧贸易的关键路线”——专访格鲁吉亚驻华大使卡岚第亚
- 助力“双减” 共筑成长——淮北市第三实验小学“小小银行家”职业初体验解锁新成长
- 直击郑州地铁五号线现场:进水口已被拦上,倒塌墙体正在抢修
- 2021城市竞争力榜单来了:“东降中升”,合肥、南昌领跑中部城市群
- 国企“触电”正当时:《国企电子商务创新发展行动计划》发布,未来5年将引领电商发展?
- 搜索